Procesos de Obtención de los Polímeros
Las clasificaciones descriptas anteriormente no son las únicas.
También, los polímeros puede clasificarse de acuerdo con el tipo de reacción química utilizada para su obtención, o la técnica de polimerización usada en la reacción química.
Estos aspectos afectan significativamente las características de los polímeros resultantes.
Reacciones de Polimerización
Las reacciones de polimerización fueron clasificadas por Carothers, en 1929, en dos grupos, de acuerdo con la composición o la estructura de los polímeros:
Reacción por Poliadición (por adición)
Ocurre en monómeros que tienen al menos un doble enlace, y la cadena polimérica se forma por la apertura de este, adicionando un monómero seguido de otro. El polímero es sintetizado por la adición de monómero insaturado a una cadena de crecimiento. Por este procedimiento se sintetizan el polietileno (PE), y las distintas poli olefinas, polímeros vinílicos y acrilicos; los poliésteres o polióxidos, como el POM (Tabla 1).
El monómero puede formar enlace o un anillo, estable químicamente y estar en estado gaseoso o líquido volátil a temperatura ambiente.
Tabla 1: Poliolfinas y polímeros vinílicos que se sintetizan por adición
Abreviatura |
Nombre |
Monómero |
|---|---|---|
PE |
Polietileno |
CH2 = CH2 |
PP |
Polipropileno |
H2C=CH–CH3 |
PS |
Poliestireno |
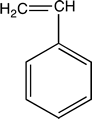 |
PVC |
Policloruro de vinilo |
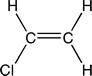 |
PAN |
Poliacrilonitrilo |
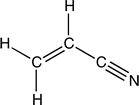 |
PMMA |
Polimetacrilato de metilo |
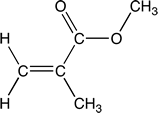 |
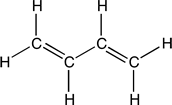
BUNA |
Polibutadieno |
 |
POM |
Polióxido de metileno |
La polimerización por adición se puede esquematizar con la serie de reacciones en cadena:
1. Iniciación I-I → 2I* (1)
2. Crecimiento 2I* +CH2 = CHX →I-CH2-C*HX (2)
3. Crecimiento R*n + monómero → R*n+1 (3)
4. Terminación R*n + R*P → Pn+p (4)
Reacción por poli condensación (por condensación): sucede entre monómeros que tienen dos o más grupos funcionales, formando adicionalmente moléculas de bajo peso molecular como agua u amoníaco (Figura 3).
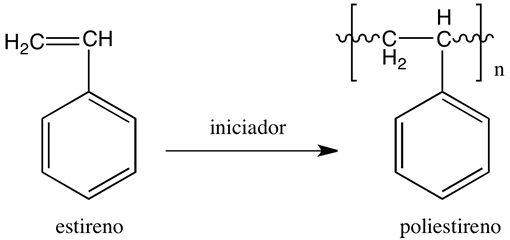
Poliadición
![]()
Policondensación
Figura 3: Reacciones de polimerización por adición y condensación.
Polimerización por condensación
La polimerización por condensación exige moléculas distintas, bifuncionales y reactantes, en proporción estequiométrica, con/sin eliminación de subproducto, normalmente agua, durante la polimerización.
Las familias principales que pueden obtenerse por este procedimiento están descriptas en la tabla 2. R, R' representan grupos orgánicos, alifáticos o aromáticos, que facilitan un gran número de combinaciones y materiales distintos posibles dentro de cada familia (Tabla 2).
Al comparar con la polimerización por adición, hay que señalar la ausencia de iniciador, la práctica desaparición de monómeros al iniciarse la polimerización, generándose dímeros, trímeros, etc., y que el final del crecimiento se consigue al añadir moléculas monofuncionales.
Esta clasificación fue perfeccionada y generalizada por Flory en 1953, utilizando como criterio el mecanismo de reacción:
Tabla 2: Familias de polímeros que se sintetizan por Condensación.
Reactantes |
Polímero |
|
|---|---|---|
Dioles |
HOH2C - R - CH2OH |
Poliésteres |
Diácidos |
HOOC-R'-CO OH |
-R - CH2- COO - R'- |
Diaminas |
H2N - R - NH2 |
Poliamidas |
Diácidos |
HOOC-R'-CO OH |
-R-NHCO-R' - |
Dioles |
HOH2C - R - CH20H |
Poliuretanos |
Diisocianatos |
OCN - R'- NCO |
- R - CH2 - NHCOO - R'- |
2 Polimerización en cadena y en etapas
Estas corresponden a las poliadiciones y poli condensaciones respectivamente (Tabla 3).
Tabla 3: Comparación de los mecanismos de polimerización
en cadena |
en etapas |
|---|---|
El monómero y las especies propagantes pueden reaccionar entre si. |
Cualesquiera de las especies moleculares en el sistema pueden reaccionar entre si. |
| La polimerización involucra al menos dos procesos cinéticos. | La polimerización tiene solo un proceso cinético. |
| El monómero se consume progresivamente durante la reacción. | El monómero se consume en un más del 99 % al comienzo de la reacción, dejando el resto para el final. |
| La velocidad de reacción crece con el tiempo hasta alcanzar un valor máximo, en el que permanece. | La velocidad de reacción es máxima en el comienzo y decrece con el tiempo. |
| El peso molecular de los polímeros formados al inicio es elevado, y no se altera con el progreso de la reacción. | El peso molecular de los polímeros formados crece lenta y paulatinamente con el progreso de la reacción. |
| La composición química % del polímero es igual que la del monómero que lo origina. | La composición química % del polímero es diferente del monómero original. |
Polimerizaciones en cadena
Este tipo de polimerizaciones presentan varias etapas conocidas como: reacciones de iniciación, propagación y terminación que son distintas y bien definidas.
La iniciación de una polimerización: en cadena puede ser inducida por calor, por agentes químicos (iniciadores) o por radiación (ultravioleta y rayos ).
El calor o la radiación provocan la rotura de los enlaces dobles del monómero (homólisis), que dejan uniones libres (radicales libres) listas para enlazarse con otros monómeros en las mismas condiciones.
La industria emplea en gran medida iniciadores químicos, que provocan la homólisis o la heterólisis del doble enlace. Este último término se refiere a la formación simultanea de radicales libres de distinta polaridad: con cargas negativas, los aniones, y carga positiva, los cationes. Esto significa que la polimerización puede desarrollarse por medio de radicales libres, por vía catiónica o por vía aniónica, o también, por coordinación.
La polimerización radical: se refiere a la polimerización iniciada por iniciador que forma radicales libres. Si el iniciador es un catión la polimerización se denomina catiónica, y si es un anión la polimerización se dice aniónica (figura 5).
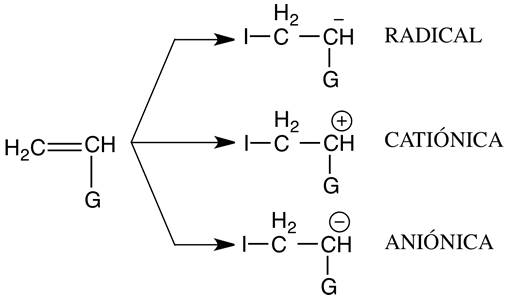
Figura 5: Reacciones de inicio de una polimerización en cadena de radicales catiónicos y aniónicos.
El caso de la polimerización por coordinación designa al hecho que los iniciadores son también catalizadores. Estos compuestos pueden estar constituidos por metales de transición o ser órgano-metálicos, como los de Ziegler-Natta.
Este tipo de catálisis se emplea con monómeros apolares, y tiene como ventaja, la obtención de polímeros altamente estéreo regulares (de estructura tridimensional regular).
La etapa propagación tiene como especie reactiva al radical libre (catión o anión) generado en la iniciación, que incorpora sucesivamente moléculas de monómero, formando la cadena polimérica (figura 6). Esta etapa de la
polimerización en cadena es muy importante, pues su velocidad influencia directamente la velocidad general de la polimerización.
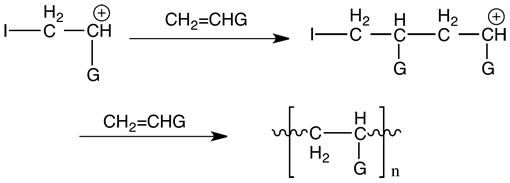
Figura 6: Propagación en una polimerización catiónica en cadena.
La terminación de la polimerización consiste en la reacción espontánea del centro activo propagante o con alguna sustancia adicionada, interrumpiendo la propagación del polímero.
La terminación de la polimerización por radícales ocurre por reacciones de combinación, desproporcionamiento o transferencia de cadena. La polimerización catiónica termina generalmente por efecto del vapor de agua u otras impurezas. Mientras que la aniónica termina cuando se añade al sistema alguna sustancia protónica (alcoholes o ácidos).
Las polimerizaciones en cadena pueden sufrir reacciones de inhibición o retardo.
La inhibición de la polimerización implica la detención de la reacción impidiendo la propagación de la cadena, que puede continuar cuando se consuma totalmente el inhibidor. Este compuesto se emplea para evitar la polimerización durante el almacenaje o el transporte. Los inhibidores más empleados son el nitrobenzeno, el m-dinitrobenzeno, la hidroquinona, el poli-t-butil-catecol, la bnaftilamina, la difenil-picril-hidrazina (DPPH) y el oxígeno.
El retardo de la polimerización ocurre cuando la velocidad de polimerización disminuye levemente por acción de retardadores.
Polimerización en etapas
Estas polimerizaciones se desarrollan por un mecanismo de repetición de la misma reacción química y a la misma velocidad. Aquí, no se diferencian las etapas de iniciación, propagación y terminación. La polimerización ocurre de forma análoga a las reacciones de algunas especies químicas de bajo peso molecular y está regida por la interferencia de impurezas, la ciclización (conversión de una molécula de cadena abierta en un compuesto cíclico) de la cadena propagante o del monómero. Ambos factores pueden disminuir significativamente la pureza del polímero resultante.
La funcionalidad del monómero determina en las polimerizaciones en etapas el polímero determina si el polímero sea lineal, ramificado, o con entrecruzamientos.
Los polímeros pueden también sintetizarse por medio de la modificación química sobre otros polímeros. Los grupos químicos de un polímero pueden reaccionar con determinadas sustancias modificándoles sus propiedades.
La obtención del poli(alcohol vinílico), PVA, es un ejemplo de la modificación química de un polímero. Este polímero se obtiene por la hidrólisis (reacción de descomposición química de una sustancia por la acción del agua) del poli(acetato de vinilo), pues no existe un monómero para el PVA.
2 Técnicas de Polimerización
Las técnicas industriales empleadas en la polimerización de un monómero son:
- La polimerización en masa.
- La polimerización en solución.
- La polimerización en suspensión.
- La polimerización en emulsión.
- La polimerización interfacial.
Cada una de estas técnicas tiene condiciones particulares que dan origen a polímeros con características diferentes (Tabla 4).
Tabla 4: Comparación de las polimerizaciones en masa, solución, suspensión y emulsión.
TIPO |
VENTAJAS |
DESVENTAJAS |
|---|---|---|
| Masa | Alto grado de pureza |
Control de temperatura difícil Distribución de peso molecular ancha |
| Solución | Control de temperatura fácil La disolución polimérica formada puede ser utilizada directamente |
El disolvente causa reducción en el peso molecular y en la velocidad de reacción Dificultades en la extracción del disolvente |
| Emulsión | Polimerización rápida Obtención de polímeros con alto peso molecular |
Fácil control de la temperatura Contaminación del polímero con agentes emulsionantes y agua |
| Suspensión | Control de temperatura fácil Obtención del polímero en forma de perlas |
Contaminación del polímero con agentes estabilizadores y agua Requiere agitación continua |
2.1 Polimerización en Masa
Esta es la técnica más simple, homogénea, donde solo el monómero y el iniciador están presentes en el sistema. La iniciación inducida por efecto térmico o por radiativo es la más económica y la que produce polímeros del mayor grado de pureza. Esta reacción es difícil de controlar térmicamente debido a que es altamente exotérmica (genera calor de formación).
Además, el polímero desde el inicio de la reacción se torna muy viscoso, dificultando la agitación necesaria para uniformar el calor en el líquido, evitando el sobrecalentamiento en determinadas zonas. Esta dificultad puede evitarse empleando inicialmente un pre-polímero (mezcla de polímero y monómero), producido a una temperatura más baja, y que conduce a una baja conversión de monómero a polímero en condiciones moderadas. La polimerización se completa por calentamiento del pre-polímero en el momento previo a la polimerización.
La polimerización en masa es muy usada en la fabricación de lentes plásticas amorfas, debido a las excelentes propiedades ópticas alcanzadas en las piezas moldeadas, sin presión, como en el caso del poli(metacrilato de metilo), PMMA.
2.2. Polimerización en Disolución
Esta polimerización requiere un disolvente para disolver al monómero y al iniciador y formar un sistema homogéneo. El solvente ideal debe tener bajo costo, bajo punto de ebullición y de fácil separación del polímero. Finalizada la polimerización, el polímero formado puede ser soluble o no en el disolvente usado.
La insolubilidad del polímero produce un barro, que puede extraíble por filtración. Si el polímero es soluble se introduce un no-disolvente para provocar la precipitación en forma de fibras o polvo.
La polimerización en solución tiene la ventaja de operar con una temperatura homogénea debido a la agitación sencilla del sistema, que evita el sobrecalentamiento. Sin embargo, el costo del disolvente y la lentitud de la reacción son inconvenientes. Esta técnica se utiliza cuando se desea aplicar la propia solución polimérica, y se emplea mucho en poli condensación.
2.3 Polimerización en Emulsión
La polimerización en emulsión es una polimerización heterogénea en medio líquido, que requiere una serie de aditivos con funciones específicas:
- Emulsionante (generalmente un detergente), taponadores de PH coloides
- Protectores
- Reguladores de tensión superficial,
- Reguladores de polimerización (modificadores)
- Activadores (agentes de reducción).
El iniciador es soluble en agua, mientras que el monómero es apenas parcialmente soluble. Esto motiva el empleo del emulsionante tiene como objetivo formar micelas, de tamaño entre 1 nm y 1 mm, formadas por el monómero. Algunas micelas son activas, pues la reacción de polimerización ocurre dentro de ellas, mientras que otras son inactivas (gotas de monómeros), siendo apenas una fuente de monómero. El progreso de la reacción provoca que las micelas inactivas sean consumidas por las activas, que crecen formando gotas de polímero, y finalmente el polímero sólido.
La velocidad de reacción y conversión es alta, y resulta sencillo el control de la agitación y la temperatura. Los polímeros obtenidos tienen pesos moleculares grades pero son de purificación compleja debido a la gran cantidad de aditivos.
2.4. Polimerización en Suspensión
La polimerización en suspensión es también llamada polimerización en perlas. La polimerización es heterogénea y el monómero y el iniciador son insolubles en agua, que actúa como medio dispersante.
La polimerización ocurre dentro de las partículas en suspensión, de 2-10 mm de tamaño medio, y que contiene el monómero y el iniciador. La velocidad de agitación determina el tamaño de las partículas. Además, el sistema cuenta con agentes tensioactivos que mantienen separadas y no adheridas entre sí las partículas y evitan su precipitación como pelas. También, este efecto se mejora con la adición de un polímero hidrosoluble de peso molecular alto, por incremento de la viscosidad del medio. Sin embargo, estas ventajas se contraponen a la dificultad para la purificación del polímero resultante.
2.5. Polimerización Interfacial
Aquí, la polimerización ocurre en la interfase entre dos solventes inmiscibles, en que cada uno de los monómeros está en una de las fases. El polímero se forma en esta interfase, luego se remueve a fin de permitir la continuidad de la polimerización. Este método es limitado a un pequeño número de polimerizaciones en etapas, debido a las condiciones de reacción necesarias.
Referencias
[Cie76] J. de la Cierva, Ed., Materiales Plásticos: Estructura y Propiedades de los polímeros; Materiales Plásticos, Elastómeros, Instituto de Plástico y Caucho Edición Extraordinaria de la Revista de Plásticos Modernos, Anuario Plásticos (Madrid) p. 3--291 (1976).
[Sh98] J. F. Shackelford, Polímeros en Introducción a la Ciencia de Materiales para Ingenieros, Prentice Hall (España) 4º ed. cap.9 p.371-401 (1998).