Antecedentes históricos
El conocimiento de la estructura atómica es fundamental para poder entender el comportamiento químico de las sustancias. El descubrimiento de las partículas subatómicas como los protones, los electrones y los neutrones, a finales del siglo XIX, impulsó a los químicos de la época a proponer modelos para explicar cómo estaban constituidos los átomos.
El primer modelo atómico fue propuesto por Thompson a finales del siglo XIX. Según Thompson, los átomos eran esferas macizas, cargadas positivamente, en las que se encontraban embebidos los electrones. Años más tarde, en 1911, un estudiante de doctorado de Thompson, llamado Rutherford, estableció el siguiente modelo atómico. Este modelo está basado en el experimento que se muestra en la figura.
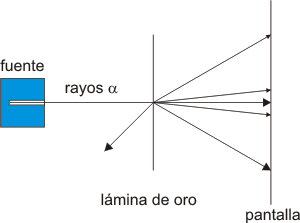
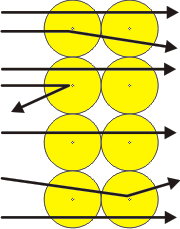
El experimento de Rutherford
Rutherford hizo pasar un haz de partículas a (cargadas positivamente y que eran emitidas por un elemento radiactivo como el polonio, Po) por una rendija, haciéndolo incidir en una lámina de oro muy delgada, de unos 400 átomos de oro de espesor. Los resultados del experimento se visualizaban en una placa fotográfica. La gran mayoría de las partículas a no sufrían desviación alguna en su trayectoria. Algunas eran desviadas un cierto ángulo y otras, muy pocas, eran fuertemente desviadas al atravesar la lámina de oro. De los resultados obtenidos en este experimento Rutherford propuso que el átomo era esférico y en su centro se concentraba toda la carga positiva y casi la totalidad de la masa atómica. Alrededor de dicho centro o núcleo giraban los electrones, de manera que el número de electrones era igual al de protones. El núcleo ocupaba, según Rutherford, un espacio muy pequeño comparado con el volumen total ocupado por el átomo, de tal suerte que éste podría considerarse prácticamente hueco. Ello explicaría que la mayoría de las partículas a no se desviaran al atravesar la lámina de oro mientras que las que sufrían desviación eran aquellas que se aproximaban al núcleo de los átomos de oro. Sin embargo, este modelo era inconsistente con los postulados de la Física Clásica: toda partícula en movimiento emite energía, por lo que la propuesta de Rutherford supondría la existencia de átomos inestables, que emitirían una radiación continua en todas las longitudes de onda.
En 1885, Balmer había demostrado que los átomos cuando emiten radiación lo hacen de forma discontinua, es decir, se obtiene un espectro discreto. Cualquier modelo atómico tendría que explicar este hecho, y el de Rutherford no estaba en concordancia con ello
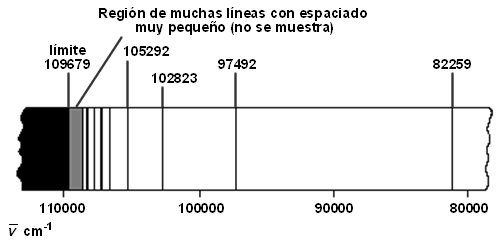
Espectro de emisión del hidrógeno
En 1913, Niels Bohr propone un nuevo modelo atómico para poder explicar la discontinuidad de los espectros atómicos y solucionar los problemas que planteaba el modelo de Rutherford. El modelo de Bohr constaba de una serie de postulados:
- El átomo está constituido por una zona central o núcleo donde se concentra toda la masa y la carga positiva del átomo.
- Los electrones giran entorno al núcleo en órbitas circulares estacionarias, de modo que Fc = Fa. (Fc = fuerza centrífuga; Fa = fuerza centrípeta).
- Los electrones sólo se mueven en órbitas estables, que son aquellas cuyo momento angular presenta un valor que es un múltiplo entero de la constante de Plank:
H = mvr = nh/2π, donde n = 1, 2, 3,... (n, número cuántico).
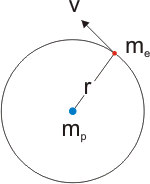
El átomo de hidrógeno de Bohr
Es decir, para Bohr el radio de las órbitas está cuantizado, de forma que el electrón no puede ocupar cualquier órbita sino aquellas que cumplan la condición señalada arriba (r = (n2h2/mZe2)). Obviamente, si las órbitas están cuantizadas las energías correspondientes a las mismas también lo estarán:
E = Ec+Ep = -(mZ2e4/2h2)(1/n2)
- Los electrones que giran en órbitas estacionarias no absorben ni emiten energía durante su movimiento. Los electrones pueden absorber o emitir energía cuando saltan de una órbita a otra de distinto radio.
La teoría atómica de Bohr explica bien la estructura del átomo de hidrógeno y su espectro electrónico, pero posee varios inconvenientes, como son, su aplicabilidad exclusiva a átomos hidrogenoides (de un sólo electrón) y el suponer una mezcla, un tanto arbitraria, de la física clásica y de la física cuántica. Por otra parte, este modelo tampoco explica el efecto Zeeman, o desdoblamiento de las líneas espectrales cuando el espectro atómico se realiza bajo la acción de un campo eléctrico. Para poder explicar estos efectos se amplió la teoría de Bohr y dando lugar al modelo de Bohr-Sommerfeld, en el que las órbitas de los electrones no sólo son circulares sino también elípticas y en ellas aparecen los números cuánticos l y m.
En 1924 De Broglie presenta su teoría denominada dualidad onda-partícula: una partícula lleva asociada siempre una onda. La longitud de onda λ (distancia entre dos máximos consecutivos de la onda) es inversamente proporcional al momento lineal p de la partícula, de acuerdo con la siguiente expresión:
λ = h/p → p = h/λ
De esta relación se deduce que cuanto mayor sea el momento lineal de la partícula menor será la longitud de onda que lleva asociada. Una consecuencia más importante de la naturaleza dual de la materia es el principio de incertidumbre de Heisemberg, enunciado en 1927. Dicho principio sostiene que es imposible especificar, simultáneamente y con exactitud, la posición y el momento lineal de una partícula, y se expresa matemáticamente de la forma siguiente:
(∆p)(∆x) ≥ h/4π
Según este principio no es posible atribuir al electrón órbitas precisas alrededor del núcleo, porque ello implicaría el conocer exactamente la posición y la velocidad del electrón en cada instante. En consecuencia, para discutir el movimiento del electrón, con una energía dada o velocidad conocida, alrededor del núcleo es necesario hablar en términos de probabilidad de encontrar a dicho electrón en una determinada posición.
La aproximación mecánico-cuántica
El concepto fundamental en el que se basa la mecánica cuántica es que la materia tiene propiedades ondulatorias. Este atributo no es evidente para objetos macroscópicos pero domina la naturaleza de partículas subatómicas como el electrón. En esta aproximación, el comportamiento de una partícula microscópica puede explicarse en términos de una función de onda, Ψ, que es una función matemática que depende de las coordenadas espaciales (x, y, z). Esta función de onda sólo describe a dicha partícula si se obtiene al solucionar la ecuación de Schrödinger, que en su forma simplificada puede escribirse como HΨ = EΨ. El término H es el operador Hamiltoniano, y engloba varios términos dependientes de cada sistema, mientras que el término E es la energía de la partícula. Así pues, cuando se aplica el Hamiltoniano a una función de onda, se obtiene la misma función de onda multiplicada por un valor E, que corresponde a la energía de la partícula definida mediante el Hamiltoniano. En realidad, el Hamiltoniano contiene dos operadores que representan la energía cinética [(-h2/8πp2m) ∇2] y la energía potencial (V) del sistema:
H = (-h2/8π2m) ∇2 + V
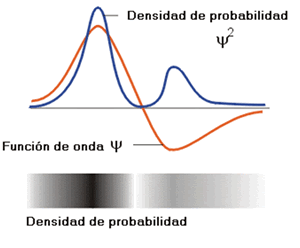
Función de onda y densidad de probabilidad
Es muy importante destacar la inexistencia de significado físico alguno de la función de onda Y. Sin embargo, el cuadrado de la función de onda es proporcional a la probabilidad de encontrar la partícula en un volumen infinitesimal del espacio. Esto se conoce como la interpretación de Born (no confundir con Bohr). En la figura anterior se representa gráficamente la función de onda Ψ así como la denominada función de densidad de probabilidad, Ψ2. De acuerdo con esta interpretación, existe una elevada probabilidad de encontrar a la partícula cuando Ψ2 es grande y la partícula no será encontrada si Ψ2 es cero. La consecuencia más importante de la interpretación de Born es la introducción del concepto de probabilidad, frente al concepto clásico de posición.
La función de onda Ψ presenta regiones de amplitud positiva y negativa. Aunque estos signos de la amplitud no tienen un significado físico directo, si resultan de gran importancia cuando funciones de onda pueden interaccionar. En este caso, las partes positivas de ambas funciones se sumarán originando un aumento de la amplitud en esa zona. Este fenómeno se conoce como interferencia constructiva. Por otra parte, si las dos funciones de onda presentan distintos signos, la parte positiva de una de ellas puede ser anulada por la parte negativa de la otra dando lugar a lo que se conoce como una interferencia destructiva. Las interferencias entre las funciones de onda suponen la base de la explicación mecano-cuántica del enlace químico.
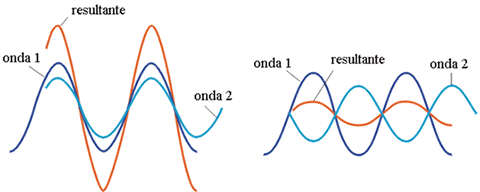
Interferencia de ondas: constructiva (izquierda) y destructiva (derecha).