La electronegatividad (c) de un elemento es la capacidad que tiene un átomo de dicho elemento para atraer hacia sí los electrones, cuando forma parte de un compuesto. Si un átomo tiene una gran tendencia a atraer electrones se dice que es muy electronegativo (como los elementos próximos al flúor) y si su tendencia es a perder esos electrones se dice que es muy electropositivo (como los elementos alcalinos). La electronegatividad tiene numerosas aplicaciones tanto en las energías de enlaces, como en las predicciones de la polaridad de los enlaces y las moléculas y, también, en la racionalización de los tipos de reacciones que pueden experimentar las especies químicas.
Por el concepto que supone, la electronegatividad se ha definido de varias formas, y aún hoy es objeto de debate. La definición original de electronegatividad de Pauling está relacionada con la energía puesta en juego cuando se forman enlaces químicos. Supóngase un enlace covalente A-B, con la energía del enlace EAB. Conociendo las energías de los enlaces A-A y B-B, se puede calcular el parámetro D como sigue:
Δ = EAB – ½ (EAA + EBB)
Este parámetro da una idea acerca de la desviación que el enlace A-B pueda tener desde una situación de enlace covalente puro. Cuanto mayor sea D, mayor será la contribución iónica a ese enlace, y en ese sentido aumenta la diferencia de electronegatividad entre ambos elementos A y B.
La definición de electronegatividad de Pauling viene dada por la siguiente expresión:
| χA - χB | = 0.102 x √Δ
Δ (kJ/mol)
La figura que se encuentra debajo muestra la variación de la electronegatividad de Pauling con respecto al número atómico, apreciándose una evolución similar a la ya observada en el radio iónico o en la energía de ionización.
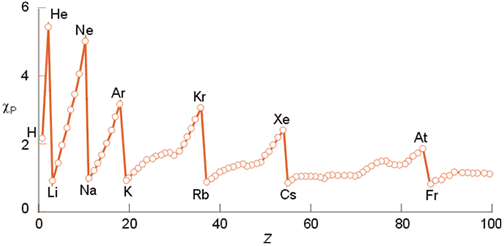
Variación de la electronegatividad (escala de Pauling) con el número atómico.
La escala de Pauling presenta algunas limitaciones, pues por ejemplo dependen del número de oxidación del elemento (la figura corresponde a los valores del máximo estado de oxidación de cada elemento). Sin embargo, esta escala es muy adecuada para calcular energías de enlace entre elementos de diferente electronegatividad así como para una visualización cualitativa de la polaridad de los enlaces.
Otra definición de esta propiedad atómica fue propuesta por Robert Mulliken al observar que cuando un elemento presenta una elevada energía de ionización, I, y una elevada afinidad electrónica, Ae, entonces presenta una gran tendencia a adquirir electrones más que a perderlos. Por ello, cuando ese elemento forme parte de un compuesto químico deberá ser bastante electronegativo. Por el contrario, cuando tanto la energía de ionización, I, como la afinidad electrónica, Ae, de un elemento tengan valores bajos, dicho elemento tendrá una marcada tendencia a perder los electrones cuando forme parte de un compuesto y, en consecuencia, será clasificado como elemento electropositivo. Estas observaciones llevaron a Mulliken a proponer su propia definición de la electronegatividad conocida como electronegatividad de Mulliken, cM, que se define como el valor medio de la suma de la energía de ionización y la afinidad electrónica de un átomo:
χM= ½ (I+Ae)
Si tanto I como Ae son elevados entonces cM tendrá también un valor alto; por el contrario si I y Ae son bajos entonces cM tendrá un valor pequeño.
Las escalas de electronegatividad de Pauling y Mulliken se pueden relacionar entre sí mediante la siguiente expresión:
χP = 1,35(√χM) -1,37
Una tercera escala de electronegatividad fue propuesta por Allred y Rochow, sobre la base de que esta propiedad viene determinada por el campo eléctrico sobre la superficie del átomo. El campo eléctrico para un sistema de este tipo debe ser proporcional a Zef/r2, lo que explica la forma de esta definición:
χAR = 0.744 + (0.3590 Zef/ r2)
donde r se expresa en Å. Las constantes numéricas se han elegido para obtener valores de electronegatividad del mismo rango que las otras escalas comentadas.