Orbital Molecular Enlazante vacuum
Por Heber Gabriel Pico Jiménez MD
Resumen
La nueva regla del octeto sostiene aquí que para que se pueda configurar un enlace químico covalente o iónico, es estrictamente necesario el debido acoplamiento electromagnético de los momentos angulares totales espín-órbita de un par de orbitales puros enlazantes, donde uno de ellos tiene que estar constituido por dos electrones apareados y de espines contrarios mientras que el otro, debe estar compuesto por un par de huecos apareados también con sus espines encontrados. Estos orbitales enlazantes generalmente se forman por efectos del canje magnético externo o ionizante que consiste en un intercambio eléctrico y reciproco de electrones por huecos efectuado por dos orbitales atómicos híbridos que son aquellos orbitales que tienen un hueco apareado a un electrón, hoy señalado como electrón desapareado. Algunos átomos que cuentan con escaso número de huecos como el nitrógeno, pues el canje magnético no ionizante no cuenta con los huecos suficientes para poder hibridar al par de electrones libres, si ese nitrógeno reacciona con átomos como el oxígeno que aun son más deficientes que él en huecos, una opción es dejar intocable a ese par de electrones libres como en los nitritos, o enfrentar al orbital puro del nitrógeno y un orbital hibrido de otro átomo de oxígeno, efectuar entre ellos un canje magnético externo que aunque ioniza al nitrógeno y al oxígeno, logra formar nitratos y es propio de la moléculas hipervalentes. Pero si ese nitrógeno reacciona con átomos como el platino que sí cuenta con suficiente cantidad de huecos, entonces ese mismo nitrógeno se porta como una base de Lewis y sin recurrir al canje magnético ionizante, configura el enlace coordinado. Para no utilizar modelos hamiltonianos aproximados, basados en una mecánica ficticia y simplificada que lo que solo busca es reproducir valores de interés particular, por eso adjuntamos el estado físico de unas partículas subatómicas que serían una forma de materia o energía oscura llamadas huecos que tienen espín, carga positiva pero no emiten suficiente radiación electromagnética para ser detectadas con los medios técnicos actuales pero cuya existencia se puede deducir a partir de la mecánica que adoptan los orbitales en los canjes magnéticos. Por esto sostenemos además que la deslocalización electrónica es aquel fenómeno que es originado por la configuración de enlaces químicos deficientes en la cantidad de orbitales enlazantes puros en huecos, en el que dos orbitales enlazantes puros en electrones que pertenecen a dos enlaces químicos contiguos y distintos, comparten de acople intermitente el mismo orbital enlazante puro en huecos, pues le toca a este par de huecos trabajar como parejas de acople temporal en los dos enlaces ubicados en lugares distintos del mismo grupo funcional o de la propia molécula. Esto sucede por ejemplo en los enlaces de hidrógenos, en la base conjugada del acido carboxílico, en los enlaces peptídicos, en las moléculas hipervalentes, en los aromáticos y en los compuestos nitroderivados. El apareamiento de las bases nitrogenadas del DNA se debe a la deslocalización externa que tienen los pares de huecos, originado por un gradiente electrostático que es ocasionado por la deslocalización electrónica interna del anillo de cada base nitrogenada, creando la circulación externa de orbitales enlazantes vacíos a través de los puentes de hidrógeno. El orbital enlazante vacío explica aquí con esto la razón del porqué el puente de hidrógeno es un enlace parcialmente covalente.
Palabras claves: Impedimento Estérico, Orbital Molecular, DNA, Huecos.
Abstract
Thanks to the new rule of byte, it is predicted that a chemical bond can be configured, is necessary because mesh that makes a couple of orbital enlazantes where one of them must be composed of two paired electrons and the other supposedly vacuum corresponds to a pair of holes also paired as different subatomic particles. The orbital two that assemble a chemical bond differ also in the location of each orbital, which are usually full of electrons are located between the atoms that originate the respective chemical bond while the empty orbital ordinarily move by the functional group or the entire molecule. The orbital empty enlazantes are the cause of the tautomerism and aromatization in bases of the nucleic acids, because they tend to uncoupling of its orbital original linking and occupied, to mate with another pair of electrons different who formerly had been an orbital antienlazante full to become after their new coupling of orbital occupied linking. The relocation of the orbital linking vacuum, explains the resonance of the conjugate base of much better than the so-called electronic delocalization carboxylic acid. When the orbital is needed linking vacuum as in hipervalentes links, even if the presence of the pair of electrons cannot be the full configuration of the respective chemical bond leaving just the molecule with the simple effects of ionic electrostatic interaction by the attraction that makes the ligand towards you on the orbital occupied antienlazante. In the DNA the orbital empty enlazantes how orbital molecular are borne the entire molecule of the nitrogenous base far ends their respective sugar, site where the steric hindrance that the atoms of oxygen in the steric form imposed on you.
Keywords: Molecular Orbital, steric hindrance, DNA, hollow.
1. Introducción
Precisamos que la introducción de todos estos artículos son iguales, debido que el objetivo es sostener la nueva regla del octeto. Es la misma introducción de los dos últimos artículos referidos a la configuración electrónica y la posición del hidrógeno en la nueva tabla periódica. En este trabajo es básico el trabajo Anomalías de configuración electrónica.
2. Desarrollo del Tema.
Entendiendo el concepto de orbital, no simplemente como aquellas funciones de ondas matemáticas de alguna ecuación en especial, que aunque si describen el comportamiento ondulatorio que pueden tener los electrones en el átomo y las moléculas, no son suficientes en la práctica para describir los sistemas físicos de las partículas, no señor, en la nueva regla del octeto entendemos como orbital molecular es al hecho físico de sorprender directamente como partículas subatómicas a un electrón o a un hueco en una determinada orbita del espacio atómico o molecular.
Tras esto se asume un estado físico de huecos que cuentan con materia oscura, carga eléctrica positiva y su respectivo espín, además se entiende que no pueden existir orbitales que no representen trayectoria de partículas algunas.
Estamos de acuerdo que los orbitales reales moleculares se construyen por combinación de los orbitales atómicos.
Es indiscutible que los orbitales moleculares describen la distribución electrónica en el campo eléctrico generado por los respectivos núcleos atómicos.
Una característica muy interesante para mostrarse de acuerdo de conferirles propiedades de partículas subatómicas a los huecos en la nueva regla del octeto, es el reconocimiento que hace la mecánica cuántica de que el número preciso de orbitales atómicos que se solapan en una molécula, es el mismo número de orbitales moleculares que resultan en la determinada molécula.
Un argumento de excepcionales pruebas para la teoría de la nueva regla del octeto, es el reconocimiento académico que han tenido los llamados orbitales moleculares antienlazantes vacíos.
Otro reconocimiento de la mecánica cuántica que prueba a la nueva regla del octeto, es el concepto de canje o intercambio magnético.
Para entregar pruebas de lo cierto de esta teoría de la nueva regla del octeto, comenzamos describiendo a los orbitales moleculares más simples que son los relacionados con la molécula de hidrógeno H2.
CONFIGURACION DEL ORBITAL ATÓMICO EN EL ÁTOMO DE HIDRÓGENO.
El átomo de hidrógeno como elemento tiene de manera natural ya híbrido a su único orbital atómico, ocupado por un único electrón identificado convencionalmente en el orbital atómico por el exponente de color azul, ubicado en el único subnivel s y además en la nueva regla del octeto este orbital híbrido está preparado para efectuar el canje magnético con el orbital también híbrido pero de otro átomo porque ese electrón, está apareado de forma fundamental con un hueco, también de valencia como una partícula, identificado convencionalmente ese hueco en el único orbital atómico con el exponente de color rojo.
Hidrógeno
1s1-1
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL HIDRÓGENO MOLECULAR H2.
Partiendo de que el átomo de hidrógeno tiene un solo orbital atómico y un solo electrón apareado con un hueco, entonces por lógica, si ese orbital consistiera solamente en la presencia solitaria de un electrón y la simple falta material de otro electrón y ese hueco, no tuviera características físicas especiales de partícula, entonces la molécula de hidrógeno debería resultar con un solo orbital que sería el orbital σ (sigma) enlazante totalmente lleno y ocupado por los dos electrones respectivos que estarían apareados y con espines contrarios.
Resulta, que si los huecos no conservaran propiedades físicas especiales de partícula todo debería quedar así, pero por efecto de que la cosa no queda de esa manera y persiste experimentalmente la presencia física de otro orbital molecular sin electrones, que aparentemente se encuentra vacío pero de electrones.
Ese otro orbital molecular que resulta en la molécula de hidrógeno hoy es llamado como un orbital σ (sigma) antienlazante vacío, a quien además de registrarle mayor cantidad energética, se le reconocen efectos estabilizadores en la respectiva molécula. Ese orbital antienlazante vacío prueba de que en realidad lo que hubo fue un canje entre los dos orbitales atómicos híbridos originales.
Los dos orbitales moleculares en la molécula de hidrógeno molecular H2, quedan representado de la siguiente manera:
1ss1-1
1ss1-1
Ó
1ss2
1ss2
La nueva regla del octeto sostiene que el reconocido orbital antienlazante vacío de la molécula de hidrógeno, quien estaría configurado por el apareamiento de un par de huecos que proceden originalmente de cada uno de los dos hidrógenos, además con cargas positivas con respecto a las cargas negativas de los electrones, entonces se forma ese orbital que no es antienlazante, que es rechazado por los dos núcleos atómicos y cuyo objetivo, es de ubicarse en alguno de los dos orbitales atómicos originales para romper la simetría eléctrica de la molécula, pero en el hidrógeno molecular es rechazado por los núcleos positivos también y no le toca sino ubicarse transversal al orbital enlazante lleno y dejar que los espines nucleares escuetos se encarguen ellos mismos de fortalecer los efectos del orbital enlazante lleno quien precisamente estaría configurado por el apareamiento de un par de electrones con espines contrarios.
El nuevo concepto de la nueva regla del octeto es que en la molécula de hidrógeno, hay dos orbitales enlazantes productos del canje magnético y donde uno de ellos está lleno de electrones y el otro, está sin electrones pero lleno de huecos como partículas subatómicas.
Por esta anterior razón en la molécula de dihidrógeno, existen dos tipos distintos de moléculas diatómicas que difieren en el tipo de relación que hay entre los respectivos espines de sus núcleos desnudos.
A este grupo pertenecen las moléculas diatómicas de flúor F2, O2, N2, Cl2, I2.
CONFIGURACION DEL ORBITAL MOLECULAR DEL CATIÓN HIDRÓGENO H+ O HIDRÓN.
Hablamos de orbital molecular en este ión llamado también protón o hidrogenión, porque es un átomo de hidrógeno que en alguna molécula ha perdido su electrón, pero por el canje magnético ha adquirido un par de huecos por lo tanto, ha quedado con un solo orbital enlazante vacío compuesto por un par de huecos apareados. El protón sin huecos jamás podrá existir solitario, sin huecos ni electrones.
1s1-1
Ó
1s2
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL CATIÓN DIHIDRÓGENO H2+.
El catión dihidrógeno H2+ está compuesto por dos protones con cargas positivas, un electrón con carga negativa y según la nueva regla del octeto hay un hueco con carga positiva apareado a ese único electrón por lo tanto el único orbital sigue siendo híbrido.
El catión dihidrógeno se forma en la naturaleza, por la ionización de una molécula de hidrógeno molecular, a través de la interacción de los rayos cósmicos.
Las partículas de los rayos cósmicos tienen suficiente energía para sacar de la molécula a un electrón pero lo sacan apareado con un hueco porque resulta que según la nueva regla del octeto, los electrones jamás pueden viajar solos sino siempre lo harán apareados con un hueco.
En la molécula de hidrógeno los rayos cósmicos dejan de la siguiente manera al único orbital molecular en el catión dihidrógeno H2+.
1ss1-1
En el catión dihidrógeno H2+ no hay presencia del orbital molecular enlazante vacío ya que el único orbital enlazante está semilleno o híbrido.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL CATIÓN DE HIDRÓGENO MOLECULAR PROTONADO H3+.
El catión de hidrógeno molecular protonado queda compuesto por tres protones, dos electrones apareados en el único orbital molecular enlazante lleno y dos huecos también apareados que cristalizan la presencia de un orbital enlazante vacío.
En el catión de hidrógeno molecular protonado H3+ quedan los dos siguientes orbitales moleculares: uno enlazante lleno y el otro también enlazante pero vacío.
1sss1-1
1sss1-1
Ó
1sss2
1sss2
En el catión de hidrógeno molecular protonado H3+, los 3 protones desnudos al lado y lado del orbital molecular enlazante vacío, aunque se repelen por tener la misma carga eléctrica, se atraen por la fuerza de la organización orto y para de los espines, al igual de lo que sucede en la molécula de hidrógeno H2.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL BORANO BH3.
El átomo de Boro tiene según la nueva regla del octeto la siguiente configuración electrónica:
[He]
2s22p11-12p222p32
Por lo tanto el Boro tiene a dos electrones apareados en el único orbital 2s y un solo electrón en el orbital híbrido de origen natural 2p1 apareado con un hueco sin embargo, hay dos pares de huecos apareados en los dos orbitales atómicos 2p2 y 2p3.
Al llevarse a cabo un canje magnético interno entre los orbitales 2s2 y 2p22 puro o no desapareados del mismo átomo de Boro y podrá adquirir la siguiente configuración electrónica con dos orbitales híbridos adicionales para un total de 3 orbitales híbridos:
[He]
2s1-12p11-12p21-12p32
Este átomo de boro con esta anterior configuración electrónica, podrá construir 3 enlaces covalentes completos con 3 átomos de hidrógenos y le quedará un orbital que tiene a un par de huecos apareados.
El borano BH3, tiene entonces a 3 orbitales moleculares enlazantes llenos, ocupados cada uno de ellos por un par de electrones apareados de espines contrarios, también tiene a 3 orbitales moleculares también enlazantes pero vacíos en electrones conformados cada uno de ellos por un par de huecos apareados como partículas y además existe finalmente un orbital 2p32 antienlzante vacío. Un total de 7 orbitales.
2ss1-1
2sp11-1
2sp21-1
2ss1-1
2sp11-1
2sp21-1
2p31-1
Ó
2ss2
2sp12
2sp22
2ss2
2sp12
2sp22
2p32
Podemos notar que en el borano BH3, cada orbital molecular enlazante que está totalmente lleno, tiene su respectivo orbital enlazante vacío, sin embargo existe un orbital que si es antienlazante vacío adicional, que es el orbital que le da las características de ácido de Lewis al borano y al diborano y además, es el orbital molecular antienlazante que al inclinar la molécula le confiere al borano las características de ser un orto o para borano, de acuerdo a la relación que tengan los espines de los 3 núcleos escuetos de los hidrógenos.
En el borano BH3, los espines nucleares de los protones de los 3 átomos de hidrógeno, quedan totalmente desnudos al igual que quedan los dos núcleos de hidrógenos en el hidrógeno molecular y los tres núcleos del hidrógeno en el reconocido hidrógeno molecular protonado H3+.
Ese par de huecos en el orbital molecular antienlazante 2p32, es el que genera la posible configuración del orto-borano o para-borano.
En el orto-borano, la dirección de espín en el hidrógeno orto, es perpendicular al plano construido con el boro por el alineamiento de los espines de los otros dos hidrógenos.
En el orto-borano, el boro mantiene 6 orbitales enlazantes, 3 son totalmente llenos de electrones con enlaces tipos 2c-2e, dos con los dos hidrógenos terminales de espines alineados en un plano con el boro y otro orbital enlazante también 2c-2e lleno con el hidrógeno que tiene espín perpendicular o hidrógeno orto. Hay 3 orbitales enlazantes vacíos.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL DIBORANO
Hasta ahora casi todo el mundo trata de definir al diborano, es con los 3 centros B-H-B haciendo puente entre los dos boranos, concibiéndolos así como enlaces de tres centros y dos electrones (3c-2e).
Sin embargo, por el hecho de que en el borano BH3, los dos electrones del orbital enlazante con el hidrógeno orto, están apareados, pensamos que la realidad es otra, que los tres centros vociferados en el enlace 3c-2c son B-H-H. De esa manera se sigue respetando el apareamiento de los electrones que constituyen el orbital enlazante del hidrógeno orto, pues no se rompe.
Se puede mirar esta situación como un enlace de 3 centros con dos electrones 3c-2e pero, la esencia del enlace entre los dos boranos, son el juego de los espines complementarios de los dos hidrógenos orto de cada borano en particular, para formar al diborano.
Podemos decir que el diborano está constituido por dos boranos recíprocamente protonados.
Los orbitales moleculares del diborano son 14 en total es decir, el diborano tiene dos veces la cantidad de orbitales moleculares que tiene el borano, 2 de ellos son orbitales moleculares antienlazantes vacíos y los 12 restantes son orbitales enlazantes donde la mitad están compuestos cada uno por un par de electrones apareados y el resto por un par de huecos apareados.
Los dos orbitales enlazantes con dos electrones apareados que están enlazando igual que en el hidrógeno molecular protonado, a 3 centros que son a los dos núcleos escuetos de los hidrógenos de transición procedente de cada borano, con un boro al lado y lado del par de núcleos de hidrógenos.
En el hidrógeno molecular protonado H3+, el único orbital enlazante lleno con tres centros está rodeado por los 3 núcleos desnudos de hidrógenos mientras que en el diborano, los dos orbitales enlazantes llenos con tres centros, están enlazando a los mismos dos núcleos de hidrógenos pero cada uno por un lado distinto a un átomo distinto de boro.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL ION HIDRONIO U OXONIO H3O+.
El átomo de oxígeno tiene según la nueva regla del octeto, la siguiente configuración electrónica:
[He]
2s22p122p21-12p31-1
Por lo tanto al cumplir la regla de Hund, el átomo de oxígeno no tiene que sufrir ninguna interacción de canje magnético interna dentro de él, porque los dos orbitales 2p2 y 2p3 son híbridos para efectuar el canje magnético externo de los enlaces químicos porque cada uno de ellos está apareado con un hueco, identificados como electrones 2p2 y 2p3.
El ion hidronio u oxonio, tiene una configuración de orbitales moleculares muy parecida al borano con la diferencia de que este último es una molécula neutra, el orbital antienlazante vacío del borano no está lleno de electrones y el elemento central en el borano es el átomo de boro mientras que en el hidronio el centro es el oxígeno. También se diferencian en que el orbital antianlazante lleno en el oxígeno del hidronio es un orbital s y no un p3 como el antienlazante vacío del boro en el borano.
El hidronio tiene el mismo número de orbitales moleculares que tiene el borano, ambos tienen el mismo número de orbitales enlazantes llenos y vacíos, tienen la misma cantidad de orbitales antienlazantes y la misma cantidad de átomos de hidrógenos.
2sp11-1
2sp21-1
2sp31-1
2sp11-1
2sp21-1
2sp31-1
2s1-1
Ó
2sp12
2sp22
2sp32
2sp12
2sp22
2sp32
2s2
Para poder configurar los orbitales llenos y vacíos de uno de los 3 enlaces covalentes del H3O+ hidronio, el orbital lleno es aportado por el oxígeno de una molécula de agua H2O y el vacío, lo facilita totalmente el ión hidrogeno H+ como ácido de Lewis que es.
El único orbital antienlazante lleno del H3O+, es totalmente aportado por el átomo de oxígeno de la molécula de H2O.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL ANIÓN HIDRÓXIDO HO-.
El anión hidróxido es una molécula que tiene dos orbitales enlazantes, uno lleno y otro vacío pero además tiene 3 orbitales antienlazantes también totalmente llenos, para un total de 5 orbitales moleculares.
2sp11-1
2sp11-1
2s1-1
2p21-1
2p31-1
Ó
2sp12
2sp12
2s2
2p22
2p32
El orbital enlazante vacío del HO-, está desplazado hacía el polo negativo del átomo de oxígeno, dejando al protón mucho más adherido y atraído al oxigeno porque está huérfano sin el par de huecos, que es de la única manera que él se pueda desprender debido a que sin huecos él no puede liberarse ya que ha quedado huérfanos de ellos.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN LA MOLÉCULA DE FLÚOR
El átomo de flúor tiene según la nueva regla del octeto la siguiente configuración electrónica:
[He]
2s22p122p222p31-1
Por lo tanto tiene un solo electrón 2p3 apareado con un solo hueco, que por esto es el único electrón que podrá formar los orbitales enlazantes necesarios en la posterior molécula de flúor.
La molécula de flúor, aparte de los 3 orbitales antienlazantes llenos, tendrá dos orbitales moleculares adicionales: uno de ellos será el orbital enlazante lleno que está compuesto por el apareamiento de un par de electrones 2p3, el otro orbital también enlazante pero vacío en el sentido tradicional porque adolece de electrones y está compuesto por el apareamiento de un par de huecos también p3 como partículas subatómicas, cuya intención será ubicarse de regreso en los orbitales atómicos originales. La molécula de flúor tiene un total de 8 orbitales moleculares enseguida describimos solamente a 5 de ellos ya que faltan 3 pero son idénticos a los 3 últimos.
2p3p31-1
2p3p31-1
2s1-1
2p11-1
2p21-1
Ó
2p3p32
2p3p32
2s2
2p12
2p22
El orbital enlazante vacío de la molécula de flúor, como tiene carga positiva semejante a la carga eléctrica contraria que tendría un par de electrones que estuvieran apareados en un orbital idéntico, entonces ese orbital es atraído por los electrones de los orbitales antienlazantes llenos, cuando ese par de huecos ocupe a uno de los orbitales atómicos originales, se pierde al instante la simetría eléctrica de la molécula y los átomos de flúor se atraen, fortaleciendo los efectos de los orbitales enlazantes, esta situación fluctúa en uno u otro sentido y se convierte en una frecuencia vibratoria de la molécula.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN LA MOLÉCULA DE OXÍGENO TRIPLETE
La molécula más estable es la de oxígeno triplete por varias razones, primero porque los dos orbitales moleculares los formaría el par de electrones 2p2 que son los electrones y huecos de menor energía.
La molécula de oxígeno triplete, además de los dos orbitales antienlazantes puros o llenos de electrones tiene un orbital también antienlazante pero es híbrido o semilleno en cada oxigeno que le confiere las calidades de paramagnético, tendrá dos orbitales moleculares enlazantes adicionales: uno de ellos será el orbital enlazante puro que está compuesto por el apareamiento de un par de electrones 2p2, el otro orbital que tendría sería un orbital enlazante también puro pero vacío, compuesto por el apareamiento de un par de huecos también 2p2 como partículas subatómicas.
Ese orbital enlazante vacío ocuparía a uno de los dos orbitales atómicos originales que precisamente forman al orbital enlazante, rompen la simetría eléctrica de la molécula y fortalecen al orbital enlazante del oxígeno triplete.
El oxigeno triplete tiene un total de 8 orbitales moleculares pero solo vamos a describir a 5 de ellos y faltarían 3 más del otro oxígeno que son idénticos a los 3 últimos.
2p2p21-1
2p2p21-1
2p31-1
2p11-1
2s1-1
Ó
2p2p22
2p2p22
2p31-1
2p12
2s2
CONFIGURACIÓN DE ORBITALES MOLECULARES EN LA MOLÉCULA DE OXÍGENO SINGLETE
El oxígeno singlete a pesar de que es una molécula con dos enlaces covalentes, es menos estable que el triplete primero porque en ella los orbitales antienlazantes vacíos, no pueden permanecer juntos en el mismo núcleo que es la única manera de romper la simetría eléctrica para fortalecer a los dos orbitales enlazantes, se repelen demasiado y entonces deben repartirse en los núcleos atómicos y eso genera mayor repulsión eléctrica entre ellos.
La molécula de oxígeno singlete, a pesar de que adolece del orbital antienlazante semi-lleno del triplete presenta los dos orbitales antienlazantes llenos en cada oxígeno del mismo, pues además de ellos tendrá 4 orbitales moleculares adicionales: 2 de ellos serán orbitales enlazantes llenos cada uno compuesto por el apareamiento de un par de electrones p2 y p3, los otros 2 orbitales que tendría serían enlazantes vacíos, compuesto cada uno por el apareamiento de un par de huecos también p2 y p3 como partículas subatómicas.
El oxígeno singlete tiene un total de 8 orbitales moleculares aquí solo describiremos los cuatro enlazantes.
2p2p21-1
2p3p31-1
2p2p21-1
2p3p31-1
Ó
2p2p22
2p3p32
2p2p22
2p3p32
CONFIGURACIÓN DE ORBITALES MOLECULARES EN LA MOLÉCULA DE NITRÓGENO
El átomo de nitrógeno tiene según la nueva regla del octeto, la siguiente configuración electrónica:
[He]
2s22p11-12p21-12p31-1
Por lo tanto al cumplir la regla de Hund, tiene los 3 electrones p híbridos porque cada uno de ellos, tiene a un electrón apareado con un hueco, identificados como electrones 2p1, 2p2 y electrón 2p3. Además de eso el átomo de boro tiene al orbital 2s totalmente puro porque tiene a dos electrones apareados y ese elemento no tiene más huecos para hibridar a esos dos electrones.
La molécula nitrógeno molecular es muy estable por varias razones, primero porque tiene 3 orbitales moleculares enlazantes compuestos por 3 pares de electrones p1, p2 y p3.
La molécula de nitrógeno además de que tiene un solo orbital antienlazante lleno por cada nitrógeno, tendrá 6 orbitales moleculares adicionales: 3 de ellos serán orbitales enlazantes llenos, cada uno compuesto por el apareamiento de un par de electrones p, los otros 3 orbitales son orbitales enlazantes vacíos, compuestos cada uno por el apareamiento de 3 pares de huecos también p como partículas subatómicas.
Esos orbitales antienlazantes vacíos mantienen la molécula siempre polarizada moviéndose entre los 3 orbitales atómicos originales que precisamente forman al orbital enlazante, rompen la simetría eléctrica de la molécula y fortalecen al orbital enlazante de la molécula de nitrógeno.
La molécula de dinitrógeno tendrá un total de 8 orbitales moleculares aquí solo describiremos los enlazantes y faltarían los antienlazantes llenos tipo s que son dos.
2p1p11-1
2p2p21-1
2p3p31-1
2p1p11-1
2p2p21-1
2p3p31-1
Ó
2p1p12
2p2p22
2p3p32
2p1p12
2p2p22
2p3p32
CONFIGURACIÓN DE ORBITALES MOLECULARES DEFICIENTES EN LA CANTIDAD DE HUECOS CON RESPECTO AL NÚMERO DE ELECTRONES
Cuando se solapan dos orbitales atómicos semi-llenos, donde el número de electrones es igual al número de huecos como hemos visto hasta el momento en este trabajo, siempre resultarán dos orbitales enlazantes configurándose ya sea enlace covalente o un enlace iónico, donde es una regla que uno de los orbitales moleculares enlazantes estará completamente lleno y el otro, será un orbital también enlazante de los que tradicionalmente se les llaman vacíos pero, son los orbitales moleculares compuestos de un par de huecos apareados como partículas subatómicas.
Estos mismos orbitales moleculares también resultarán si se solapa un orbital atómico lleno y el otro esté como se dice tradicionalmente totalmente vacío. En este caso se configurará un enlace de coordinación.
Pero cuando se solapan dos orbitales atómicos donde uno está lleno y el otro híbrido o semilleno, es decir el número de electrones es mayor que el número de huecos, entonces para que se alcance el equilibrio y se formen orbitales moleculares, se hace necesario la intervención al mismo tiempo de por lo menos otro orbital atómico, que no podría estar totalmente lleno ni vacío, necesariamente tendría que estar híbrido también o semi-lleno.
Intervendrán 3 orbitales atómicos: uno de ellos estará totalmente lleno y dos de los orbitales participes estarán semi-llenos o híbridos.
Como participan 3 orbitales atómicos, entonces respetando la regla, deben surgir también 3 orbitales moleculares enlazantes, dos orbitales enlazantes estarán llenos y solo uno de los 3 orbitales será un enlazante tradicionalmente vacío.
Entonces se configurará y estamos en presencia, de un enlace hipervalente que es un enlace descrito como de 3 centros y 4 electrones.
ENLACES DE TRES CENTROS CON CUATRO ELECTRONES
Los enlaces de 3 centros con 4 electrones son ejemplo de enlaces deficientes en el número de huecos con respecto a la cantidad de electrones. Una de las moléculas con deficiencia de huecos o excesos relativos de electrones, son enlaces que las que los tienen moléculas conocidas como hipervalentes.
El dilema de este enlace es que a pesar de que se originan 2 orbitales enlazantes llenos resulta un solo orbital molecular enlazante vacío sin electrones.
Debido a que el orbital enlazante vacío está constituido por huecos, entonces en las moléculas hipervalentes no queda sino un solo orbital con un solo par de huecos apareados en el único orbital enlazante tradicionalmente vacío acoplando a dos orbitales enlazantes llenos.
El problema radica en que el átomo central no tiene huecos para poder efectuar un canje magnético interno para hibridar los dos electrones del orbital s que él ofrece a los dos ligandos está lleno, con dos electrones apareados de espines contrarios del cual se originan los dos orbitales moleculares con los dos ligandos. El hueco que tienen apareados cada ligando con cada uno de sus respectivos electrones, originado por un orbital híbrido o semilleno, quienes forman un solo orbital enlazante donde yacen un par de huecos apareados. Esta es la razón por la cual los dos ligandos terminales son altamente electronegativos, ya que ellos solos aportan sus dos huecos con carga positiva.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL ANIÓN FOSFATO PO43-.
Hemos escogido esta molécula hipervalente por lo esencial que es para la vida, por su papel en los ácidos nucleídos, en el almacenamiento de energía y su labor de soporte estructural en la transmisión de señales de los fosfolípidos en las membranas celulares activas.
Las configuraciones electrónicas del átomo de oxígeno y el átomo de fósforo son las siguientes.
Oxígeno
[He]
2s22p122p21-12p31-1
Fósforo
[Ne]
3s23p11-13p21-13p31-1
El átomo de fósforo, tiene 4 orbitales de valencia y los orbitales 3p1, 3p2 y 3p3 son orbitales hibridados de forma fundamental a través de la regla de máxima multiplicidad de Hund y el orbital 3s, no es híbrido porque tiene en su seno a un par de electrones apareados, el átomo de fósforo no tiene más huecos para poder efectuar un canje magnético interno que le permita de por sí hibridar a esos dos electrones del orbital 3s y la única opción que le queda en el PO43- es recurrir a un enlace coordinado o efectuar canje magnético externo con un ligando de oxígeno, para configurar enlaces hipervalentes.
El primer paso para formar el anión PO43- lo hace el fósforo, cuando efectúa un canje magnético externo con un átomo de oxígeno para convertirse en el ión P+. Este ión de fósforo híbrida así a los 4 orbitales de valencia y quedan el fósforo y el oxígeno O- del canje con la siguiente configuración electrónica:
Oxígeno
[He]
2s22p122p222p31-1
Fósforo
[Ne]
3s1-13p11-13p21-13p31-1
El ión P+ queda con carga positiva porque el fósforo neutro entrega un electrón y recibe un hueco del oxígeno convirtiéndose en un catión o ión positivo. Los 4 orbitales del fósforo 3s1-1, 3p11-1 y 3p31-1 quedan híbridos, cuestión que lo deja apto para formar cuatro enlaces covalentes con 4 iones O- distintos de oxígeno.
El oxígeno queda con doble carga negativa por entregar un electrón negativo y recibir un hueco O-.
El anión fosfato PO43- está compuesto por un catión central de fósforo, que tiene a 4 oxígenos a su alrededor con idénticas ionizaciones, se forman 8 orbitales enlazantes, 4 llenos y 4 vacíos, que configuran a 4 enlaces covalentes entre el fósforo central y los 4 átomos distintos de oxígenos, dispuestos tetraédricamente a su alrededor.
2p23p11-1
2p23p21-1
2p23p31-1
2p23s1-1
2p23p11-1
2p23p21-1
2p23p31-1
2p22p21-1
Ó
2p23p12
2p23p22
2p23p32
2p23s2
2p23p12
2p23p22
2p23p32
2p22p22
En esta molécula de PO43- hay que destacar varios aspectos por ejemplo, es una molécula donde existe deslocalización de 4 orbitales enlazantes vacíos y la deslocalización también de 4 orbitales enlazantes llenos. Además cada oxígeno presenta a 3 orbitales antienlazantes llenos de alta energía. Los 4 enlaces que podían ser enlaces dobles pero en realidad lo que hay es una resonancia por la deslocalización interna del orbital enlazante vacío, entre el enlace covalente simple y la interacción iónica con dos electrones de cada uno de los 3 orbitales antienlazantes llenos de los oxígenos, interacción entre el anión oxígeno con el catión fósforo.
Es decir el orbital enlazante vacío resuena en una y otra posición pero siempre entre los mismos dos átomos de oxígeno y fósforo, pero resuenan todos dos.
Debido a la distinta electronegatividad entre el oxígeno y el fósforo, existe un desplazamiento hacía el oxígeno de los dos electrones que podrían configurar un orbital enlazante lleno de un enlace doble con el fósforo, electrones que al quedar sin orbital enlazante vacío, no alcanzan a configurar un enlace doble dejándolo con el carácter de un enlace sencillo resonante, debido a esto el fósforo se queda con carga positiva mientras que todos los oxígenos que lo rodean, quedan con cargas eléctricas contrarias a la del fósforo.
En el anión fosfato PO43-, cada oxígeno aporta a 3 orbitales antienlazantes llenos para haber un total de 12 de ellos y uno solo de estos en cualquiera de los oxígenos, hace la interacción que aparenta ser un enlace covalente pero no es así, porque le hace falta un orbital enlazante vacío.
Esa interacción interna donde hace falta un orbital enlazante vacío, se mueve de forma resonante entre los 2 enlace con cada uno de los oxígenos del PO43-.
Todo esto nos dice que el PO43- tiene un total de 20 orbitales moleculares.
Podemos decir que el PO43- tiene 4 veces el fenómeno donde hay 3 orbitales enlazantes llenos que comparten a un solo orbital enlazante vacío.
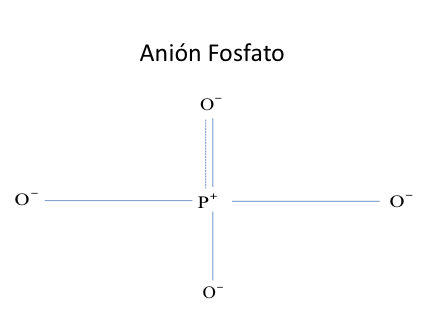
Figura No.1
En la anterior figura No.1, las líneas dobles punteadas con cada uno de los 4 oxígenos, señala la resonancia por la deslocalización del orbital enlazante vacío quien se mueve entre uno y el otro par de electrones configurando siempre a un solo enlace covalente pero, resuena entre una y otra posición.
Un solo átomo de fósforo central en el PO43- donde resuena el orbital enlazante vacío quien mantiene la carga eléctrica del fósforo, además existen 4 oxígenos cargados sin la posibilidad de que haya transferencia de electrones deslocalizados.
El PO43- es el extremo del nucleótido donde se encuentra el polo del orbital enlazante vacío.
CONFIGURACIÓN DE ORBITALES MOLECULARES EN EL ANIÓN TRIFOSFATO P3O105-.
A pesar de que en el anión PO43- , además de deslocalizados los 3 orbitales antienlazantes llenos de baja energía, tiene un solo orbital enlazante vacío deslocalizado con también un solo orbital enlazante lleno deslocalizados, al anión trifosfato P3O105- triplica esta cantidad es decir, presenta deslocalizados esta vez a 3 orbitales enlazantes vacíos en los 3 fósforo con 3 orbitales enlazantes llenos pero también deslocalizados y además tiene a 5 orbitales antienlazantes llenos aun deslocalizados.
El trifosfato multiplica por 3 las veces de la cantidad de orbitales enlazantes que tiene el anión fosfato PO43- es decir, que entonces tiene a 12 orbitales enlazantes llenos y 12 orbitales enlazantes vacíos, para un total de 24 orbitales enlazantes.
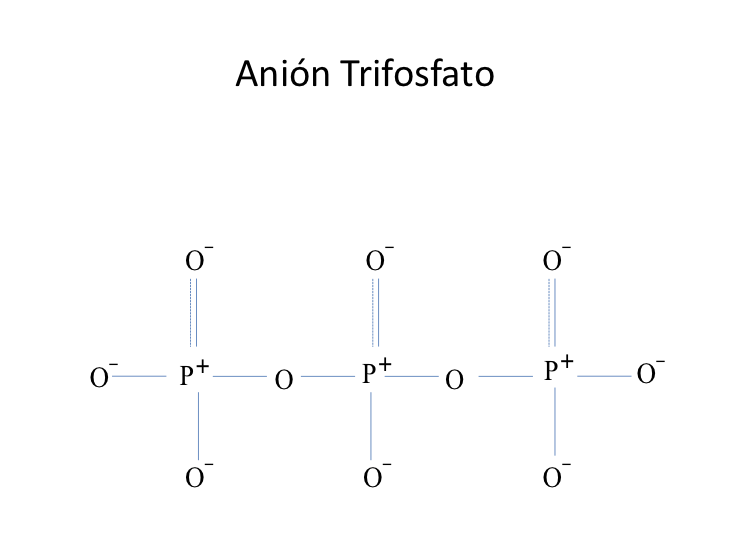
Figura No.3
ENLACES FOSFODIÉSTER
El enlace fosfodiéster son los enlaces que ayudan a aislar entre las cadenas carbonadas al aislante biológico PO43-.
Son los enlaces que ayudan con los PO43- a aislar los nucleótidos en el DNA y RNA.
Son los enlaces que ayudan al PO43- a separar la parte hidrófoba de la parte hidrofílica en los fosfolípidos.
Cuando en el radical PO43-, dos de los 4 átomos de oxígenos están ocupados por un radical carbonado como en los ácidos nucleídos, se forman los enlaces fosfodiésteres donde a la molécula le sigue haciendo falta un orbital enlazante vacío y el fósforo no forma el enlace doble pero queda resonando solamente entre dos átomos de oxígenos RRPO41-.
Esto mismo ocurre en los fosfolípidos y en el AMP cíclico, donde quedan dos átomos de oxígenos resonando la interacción electrostática entre el fosforo y uno de ellos.
Enlace fosfodiéster RRPO41-. R es un radical carbonado.
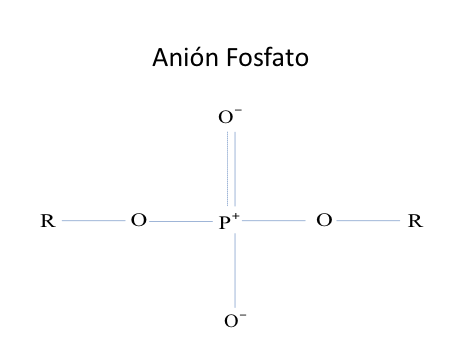
Figura No.2.
El anión RRPO41- es un ión que forma parte de la cabeza hidrófilica de los fosfolípidos.
En el enlace fosfodiéster ya el par de electrones de cada oxígeno han dejado de ser electrones deslocalizados y por lo tanto son enlaces que bloquean el flujo de electrones y de huecos.
CANJE MAGNÉTICO EXTERNO EN EL NITRÓGENO
El átomo de nitrógeno utiliza también las mismas hibridaciones del fósforo 2s1-1, 2p11-1 y 2p31-1 por ejemplo, usa a los 4 orbitales híbridos para formar 4 enlaces covalentes con 3 oxígenos y formar los nitratos, que tienen a 4 orbitales enlazantes puros electrónicos y 4 orbitales enlazantes vacíos puros, donde el azoe central queda con carga positiva. En los nitratos, uno de los orbitales enlazantes vacíos resuena acompañando al otro enlace químico cambiando en los 3 diferentes oxígenos. En el ácido nítrico y en los compuestos nitroderivados solo resuena en dos de los 3 oxígenos.
Esta misma hibridación es útil para reaccionar con 4 hidrógenos y formar el ión amonio NH4+ quien es una molécula iónica que tiene de positivo es el nitrógeno y no a los hidrógenos. En medio ácido y en disolución acuosa la concentración de amoniaco no permite esperar que el nitrógeno haga ese canje magnético externo del azoe.
HALOGENUROS DE FÓSFORO Y ANTIMONIO
En los pentahalogenuros de fósforo y antimonio, incluso el mismo hexafluoruro de azufre, el fósforo y el azufre como elementos centrales, buscan inicialmente más huecos externos en los ligandos, para poder hibridar sp3 a sus valencias a través de los canjes magnéticos externos.
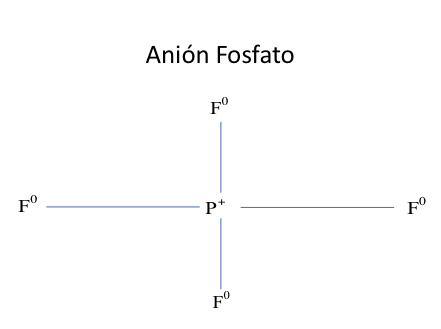
Figura No.2.
En la anterior figura, a pesar de que el fósforo continúa con la misma carga eléctrica positiva del PO43-, efectúa 4 enlaces covalentes con 4 átomos neutros de flúor o de cloro. Entonces le toca tomar el orbital enlazante vacío de uno de esos enlaces covalentes y ponerlo a resonar con el anión de flúor F- que hizo el canje magnético externo quien no tiene huecos, incluso con el antimonio puede dejar en un mismo plano a los 4 enlaces covalentes con átomos neutros de flúor y situar en un mismo eje a dos aniones de flúor, efectuando dos interacciones electrostáticas iónicas con ellos en el SbF6-.
RESONANCIA DEL OZONO, EL BENCENO Y EL CATIÓN DEL GRUPO ALILO
La resonancia del ozono es una molécula hipervalente debido a que el oxígeno central, primero efectúa un canje magnético externo con otro de sus oxígenos ligandos de los dos oxígenos de los extremos, tratando de hibridar al orbital 2p12 tratando de convertirlo en 2p11-1.
Oxígeno
[He]
2s22p122p21-12p31-1
Esta distribución electrónica anterior es un átomo neutro de oxígeno fundamental cumpliendo solo a la regla de Hund. Cuando este átomo central efectúa el canje magnético externo del orbital 2p12 de él con el orbital híbrido 2p11-1 de otro oxígeno, quedan dos oxígenos ionizados, uno central con carga positiva O+ donde los 3 orbitales 2p1, 2p2 y 2p3 quedan hibridados, el otro es un oxígeno ligando con carga negativa O- donde solamente el orbital 2p3 es el híbrido de la siguiente manera:
Oxígeno central O+
[He]
2s22p11-12p21-12p31-1
Oxígeno extremo derecho O-
[He]
2s22p122p222p31-1
Oxígeno extremo izquierdo O0
[He]
2s22p122p21-12p31-1
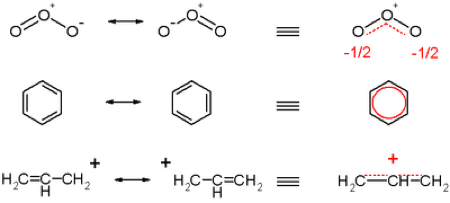
Lo que existe en todos los casos es una deslocalización de los orbitales enlazantes vacíos, que en el ozono y en el catión del grupo alilo son solo un orbital enlazante puro y vacio pero, en el benceno son 6 los orbitales vacíos deslocalizados y son enlazantes puros en huecos.
ORBITALES HÍBRIDOS
Los orbitales híbridos son aquellos que tienen apareado un electrón a un hueco. La nueva regla del octeto parte de que un orbital atómico está habitado siempre por dos partículas con espines opuestos, esas dos partículas pueden ser dos electrones o dos huecos y en ambos casos, el orbital es un orbital puro en electrones o puro en huecos. Si el orbital lo ocupa un electrón apareado a un hueco entonces se llama orbital híbrido. El hecho de ser híbrido o no es una propiedad individual del orbital.
Los orbitales atómicos pueden tener una hibridación fundamental originada por la regla de Hund o pueden adquirir la configuración de híbridos a través del canje magnético.
Hay dos tipos de hibridaciones: 1-) Las hibridaciones que ocurren a través del canje magnético interno o no ionizante que pisan terrenos propios de la regla de máxima multiplicidad de Hund. 2-) Las hibridaciones que ocurren a través del canje magnético externo o ionizante que utilizan en su formación las moléculas hipervalentes.
HIBRIDACIÓN DE ORBITALES
Cuando un orbital puro en electrones o puro en huecos, se convierte en un orbital híbrido, es porque ese orbital ha intercambiado a una de sus dos partículas con otro orbital contrario puro o por lo menos es un orbital también híbrido, esto sucede a través de un canje magnético que puede ser interno o externo y si lo hacen, de inmediato por lo menos alguno de los dos se convierte en un orbital híbrido, es decir se han hibridado. Puede ser que uno sea puro y el otro híbrido y hagan canje magnético externo como el caso de las moléculas hipervalentes.
Mientras que la condición de híbrido es individual en los orbitales, las hibridaciones si necesitan que el canje magnético se efectúe con la intervención de dos orbitales atómicos y también deben resultar dos orbitales por regla que por lo menos uno de ellos sea híbrido.
Lo nuevo de este trabajo es que en realidad, la hibridación también se puede llevar a cabo por canje magnético externo de orbitales que pertenecen a átomos distintos.
Para nombrar a los orbitales híbridos debemos identificar si son atómicos o moleculares y además, indicar su origen es decir, hay que dejar claro si son híbridos originales en el respectivo átomo o si son adquiridos por este. Cuando son orbitales híbridos adquiridos se tiene que dejar implícito el tipo de orbitales que los originan y que canjean partículas para formarlos, a ver si es un canje interno con orbitales de un mismo átomo o un canje externo si intervienen dos orbitales propios de dos átomos distintos.
INTERACCION DE CANJE MAGNÉTICO
La interacción de canje magnético, un efecto descrito por la mecánica cuántica que no ha tenido análogo clásico, pues esa misma derivación es la que nosotros describimos y definimos que es un intercambio reciproco eléctrico de electrones por huecos que se lleva a cabo entre dos orbitales independiente de que ellos sean híbridos o puros y hay dos tipos distintos del mismo fenómeno que tienen efectos que la mayoría de las veces son contrarios, ellas son: La Interacción de canje magnético interno o no ionizante y la Interacción de canje magnético externo o ionizante.
INTERACCIÓN DE CANJE MAGNÉTICO INTERNO O NO IONIZANTE: es cuando el canje magnético actúa sobre dos orbitales que generalmente ambos son puros pero también sucede cuando uno de ellos o ambos son impuros como en el platino, eso sí que esos orbitales hacen parte de los orbitales de valencia del mismo elemento, actúa con el fin de preparar el átomo para obtener el máximo número de nuevos orbitales atómicos impuros o nuevos híbridos, claro eso de acuerdo a la cantidad de electrones y huecos que tiene disponibles el referido elemento.
INTERACCIÓN DE CANJE MAGNÉTICO EXTERNO O IONIZANTE: es cuando el canje magnético se efectúa entre dos orbitales de valencia, que pueden ser híbridos o puros pero eso sí que esos orbitales de valencia correspondan a elementos distintos. La mayoría de las veces, para formar enlaces químicos este canje deshibridan a los dos orbitales de valencia híbridos. Otras veces es para configurar las moléculas hipervalentes.
Cuando reacciona una base con un ácido de Lewis, es decir un átomo que actúa con un orbital puro de valencia con dos electrones apareados en su dominio, reacciona con otro orbital atómico de valencia de un átomo distinto que tiene a dos huecos apareados en su seno, en esta situación para configurar un enlace covalente estos dos orbitales no deben efectuar un intercambio eléctrico o canje magnético externo, solo pueden coordinar un acople eléctrico entre ellos.
Cuando el canje magnético externo se efectúa entre dos orbitales de valencia de un ligandos híbridos enfrente de un orbital central de valencia puro en electrones, antes de conformar una determinada molécula, lo más probable es que la respectiva molécula formada sea hipervalente.
ENLACE DE COORDINACIÓN
El enlace coordinado es un enlace que no es ionizante y por lo tanto no tiene que recurrir a los efectos del canje magnético externo o ionizante, solo necesita es establecer el acople electromagnético entre el orbital del par de electrones y el orbital del par de huecos.
Para describir el enlace coordinado vamos a referirnos a un complejo de coordinación llamado Cisplatino:
El nitrógeno tiene 4 orbitales atómicos de valencia, un orbital ns electrónico puro y 3 orbitales np (np1, np2, np3) híbridos. El podía hibridar al orbital s pero no cuenta con más huecos, solo le queda la alternativa de poder efectuar canje magnético externo ionizante para configurar enlaces hipervalentes o configurar enlaces de coordinación sin tener que recurrir al canje magnético ionizante.
Nitrógeno
[He]
2s22p11-12p21-12p31-1
El platino tiene 24 electrones y 8 huecos de primera valencia [Xe]4f1-725d1-425d51-16s1-16p1-32 distribuidos en los orbitales atómicos de la siguiente manera:
Platino fundamental
[Xe]4f124f224f324f424f524f624f72
[Xe]5d125d225d325d425d51-1
6s1-16p126p226p32
El átomo de platino tiene un total de 16 orbitales en la primera Valencia de los cuales tres son np1-32 que son orbitales de puros huecos, uno ns1-1 es híbrido, cinco (n-1)d dentro de los cuales cuatro (4) son (n-1)d1-42 orbitales electrónicos puros mientras que uno de ellos queda hibrido (n-1)d51-1 y siete son (n-2)f1-72 orbitales electrónicos puros.
El átomo de platino tal y como está configurado electrónicamente en el aparte inmediatamente anterior, el orbital híbrido 5d51-1 y el orbital puro en huecos 6p12, efectúan un intercambio magnético interno quedando la configuración del platino de la siguiente manera:
Platino hibridado
[Xe]4f124f224f324f424f524f624f72
[Xe]5d125d225d325d425d52
6s1-16p11-16p226p32
Este átomo último de platino, tiene dos orbitales híbridos, 6s1-1, 6p11-1 que son los orbitales que efectuarán el doble canje magnético externo para deshibridarse y hacer los dos enlaces covalentes con los dos cloros. Los orbitales 6p22 y 6p32 son los dos orbitales puros en huecos que efectuarán los dos enlaces de coordinación que no utilizan canje magnético ionizante con los dos nitrógenos del amoniaco.
3- Conclusiones:
a)- LA PRIMERA EXTRAORDINARIA Y GRAN CONCLUSIÓN de este trabajo, es la resonancia ocurrida en las bases conjugadas de los ácidos carboxílicos, donde a pesar de que hay la deslocalización electrónica de un orbital enlazante lleno y de un orbital enlazante vacío, el que se mueve es el par de huecos como anti-partículas subatómicas.
Debido a que los dos oxígenos ionizados del acido carboxílico son iguales, el orbital enlazantes vacío del enlace doble del oxígeno en la base conjugada del ácido carboxílico, no sabe donde ubicarse y uno de ellos llega al átomo de carbono central y continúa hasta el otro oxígeno, donde encuentra un enlace sencillo pero con él se conforma allí un nuevo enlace doble pero como también es atraído por el otro vuelve a recorrer el camino contrario, permaneciendo más tiempo en el átomo central de carbono y como tienen carga eléctrica positiva fortalece una especie de un carbocatión primario.
Cuando el orbital enlazante vacío abandona el enlace doble en uno de los oxígenos, como el átomo de oxígeno es más electronegativo que el mismo carbono, entonces el oxígeno atrae hacía sí a los dos electrones que conforman al orbital enlazante ocupado del enlace covalente.
El orbital enlazante vacío del OH que estaba configurando al enlace simple del oxígeno con el hidrógeno, se lo lleva el hidrógeno con él para unirse a un orbital antienlazante lleno que tenía esperándolo otro oxígeno en una molécula de agua del solvente y formar así el catión H3O+.
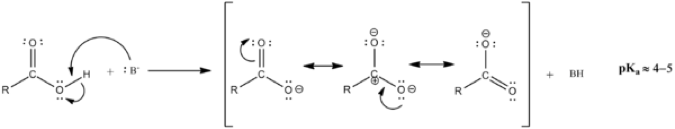
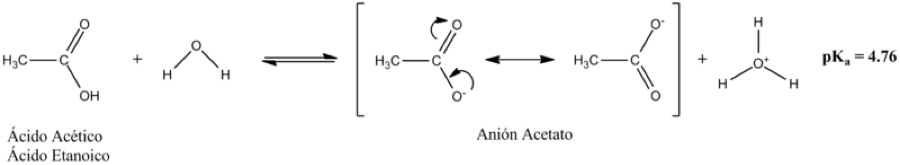
Hay una deslocalización electrónica en el grupo carboxílico, porque ambos oxígenos se quedan con los dos electrones retraídos del respectivo orbital enlazante ocupado del pertinente enlace, para convertirse en un orbital antienlazante lleno por el enlace que rompen cuando dejan de tener un enlace doble para configurar un enlace simple.
b)- LA SEGUNDA GRAN CONCLUSIÓN es que aunque tarda más tiempo en el oxígeno, de la misma manera que persiste la resonancia del orbital enlazante vacío en el ácido carboxílico, también permanece en la resonancia de los enlaces peptídicos.
Hemos traído a estas conclusiones la siguiente figura para resaltar la gran contradicción que hay en ella, cuando se trata de explicar la resonancia del enlace peptídico que es inexplicable sin la ayuda de los nuevos conceptos de la nueva regla del octeto. No sabemos cuál es el concepto autorizado de la academia en cuanto a este tema pero lo más probable es que estén llenos de incertidumbre con el contenido.
El orbital antienlace lleno que tiene el nitrógeno a la izquierda de la figura, cuando le llega el orbital enlazante vacío se convierte en un orbital enlazante ocupado y ellos dos configuran un segundo enlace químico entre el nitrógeno y el carbono. Mientras que en el oxígeno, al quedar sin orbital enlazante vacío el par enlazante ocupado de uno de los dos enlaces químicos, lo convierte en un par antienlace lleno y lo atrae hacía sí, quedándose con 3 pares de electrones libres y un enlace simple. No es necesario que los dos electrones se desplacen ni se acerquen al carbono y mucho menos al nitrógeno, por esto el oxígeno queda con carga negativa. El nitrógeno queda con carga positiva porque aporta el par de electrones para formar dos enlaces con el carbono.
c)- LA TERCERA GRAN CONCLUSIÓN es el hecho de que un efecto como la “interacción de canje magnético” haya sido detallada en este trabajo y que haya sido descrita también por la mecánica cuántica, efecto que está íntimamente relacionado con el principio de exclusión de Pauli, que es parte de la correlación electrónica y que está relacionado con lo que se conoce como hueco de Fermi, efecto que incluso no tiene análogo clásico alguno, pues ese efecto también lo relaciona este trabajo con la teoría de la hibridación de orbitales atómicos referida en la teoría del enlace de valencia.
d)- LA CUARTA GRAN CONCLUSIÓN de este trabajo es que la teoría de la hibridación que desarrolló Linus Pauling por primera vez, es el resultado del canje magnético interno que hacen los orbitales atómicos dentro de un mismo átomo.
e)- LA QUINTA GRAN CONCLUSIÓN de este trabajo es que un orbital lleno de un par de electrones apareados, es un orbital puro en electrones debido a que no es orbital híbrido.
f)- LA SEXTA GRAN CONCLUSIÓN de este trabajo es que un orbital lleno de un par de huecos apareados, es un orbital puro en huecos debido también a que no es orbital híbrido.
g)- LA SEPTIMA GRAN CONCLUSIÓN de este trabajo es que un orbital que está ocupado por un electrón que está apareado a un hueco, es un orbital híbrido y se distingue hasta ahora como un electrón desapareado.
g)- LA OCTAVA GRAN CONCLUSIÓN de este trabajo es que cuando se lleva a cabo la interacción de canje magnético externo entre orbitales de átomos diferentes, la mayoría de las veces es porque son orbitales híbridos donde se encuentra un electrón apareado a un hueco, llamados ahora electrones desapareados.
h)- LA NOVENA GRAN CONCLUSIÓN de este trabajo es que si dos orbitales puros concurren a hibridarse, pues los mismos dos resultan híbridos.
i)- LA DECIMA GRAN CONCLUSIÓN de este trabajo es que los orbitales híbridos de un átomo, reaccionan mucho antes con el canje de interacción magnética externa que los orbitales puros del mismo elemento.
j)- LA DECIMOPRIMERA GRAN CONCLUSIÓN de este trabajo es la de postular de que las únicas moléculas donde el átomo central utiliza el canje magnético externo para hibridarse, son las moléculas hipervalentes.
4- Referencias
REFERENCIAS DEL ARTÍCULO.
[1] Nueva tabla periódica.
[2] Nueva tabla periódica.
[3] Ciclo del Ozono
[4] Ciclo del Ozono
[5] Barrera Interna de Potencial
[6] Barrera Interna de Potencial
[7] Ácido Fluoroantimónico.
[8] Ácido Fluoroantimónico.
[9] Dióxido de cloro
[10]Dióxido de cloro
[11]Pentafluoruro de Antimonio
[12]Pentafluoruro de Antimonio
[13]Tetróxido de Osmio
[14]Enlaces Hipervalentes
[15]Enlaces en moléculas Hipervalentes
[16]Nueva regla del octeto
[17]Estado fundamental del átomo
[18]Estado fundamental del átomo
[19]Barrera rotacional del etano.
[20]Enlaces de uno y tres electrones.
[21]Enlaces de uno y tres electrones.
[22]Origen de la barrera rotacional del etano
[23]Monóxido de Carbono
[24]Nueva regla fisicoquímica del octeto
[25]Células fotoeléctricas Monografías.
[26]Células Fotoeléctricas textoscientificos.
[27]Semiconductores Monografías.
[28]Semiconductores textoscientificos.
[29]Superconductividad.
[30]Superconductividad.
[31]Alotropía.
[32]Alotropía del Carbono.
[33]Alotropía del Oxigeno.
[34]Ozono.
[35]Diborano
[36]Semiconductores y temperatura.
REFERENCIAS DE LA TEORÍA
[1] Número cuántico magnético.
[2] Ángulo cuántico
[3] Paul Dirac y Nosotros
[4] Numero cuántico Azimutal monografias
[5] Numero cuántico Azimutal textoscientificos
[6] Inflación Cuántica textos científicos.
[7] Números cuánticos textoscientíficos.com.
[8] Inflación Cuántica Monografías
[9] Orbital Atómico
[10] Números Cuánticos.
[11] Átomo de Bohr.
[12] Líneas de Balmer.
[13] Constante Rydberg.
[14] Dilatación gravitacional del tiempo.
[15] Número Cuántico magnético.
[16] Numero Cuántico Azimutal.
Copyright © Derechos Reservados.
Heber Gabriel Pico Jiménez MD. Médico Cirujano 1985 de la Universidad de Cartagena Colombia. Investigador independiente de problemas biofísicos médicos propios de la memoria, el aprendizaje y otros entre ellos la enfermedad de Alzheimer.
Estos trabajos, que lo más probable es que estén desfasados por la poderosa magia secreta que tiene la ignorancia y la ingenuidad, sin embargo, como cualquier representante de la comunidad académica que soy, también han sido debidamente presentados sobretodo este se presentó el 09 de Junio del 2014 en la “Academia Colombiana de Ciencias Exactas, Físicas y Naturales” ACCEFYN.