Compuestos del fósforo
El fósforo forma una gran cantidad de compuestos binarios con casi todos los elementos (excepto gases nobles, Bi y Sb), la mayor parte de las veces por reacción directa. Como el boro y el silicio, puede formar muchos compuestos de diferente estequiometría con un mismo elemento.
Por ejemplo, se conocen al menos 8 fosfuros de níquel.
Compuestos del fósforo con hidrógeno
El fósforo forma una serie de hidruros de fórmula general PnHn+2 de los cuales sólo la fosfina PH3 es estable.
Fosfina
La diferencia entre el N y P se refleja en las propiedades de sus hidruros más sencillos: el amoníaco y la fosfina. Todos estamos familiarizados con el amoníaco y reconocemos su característico olor picante, el de la fosfina recuerda al del pescado podrido. La fosfina es un gas extremadamente venenoso.
Los dos hidruros, NH3 y PH3, mantienen una cierta analogía estructural (el ángulo H–E-H es menor en la fosfina) pero difieren en cuanto a sus propiedades. El enlace P–H es apolar debido a que P y H tienen la misma electronegatividad. A pesar que el amoníaco presenta unos enlaces de hidrógeno bastante débiles ayudan a que sea 2500 veces más soluble en agua que la fosfina.
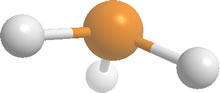
Fosfina
Esa misma apolaridad del enlace, reflejada en un momento dipolar mucho menor, justifica que, a pesar de su mayor masa molecular, la fosfina sea más volátil que el amoníaco. La fosfina líquida se autoioniza menos que el amoníaco y tiene menor tendencia a protonarse. Tampoco presenta la tendencia del amoníaco a reaccionar como un aceptor ni dador de protones.
Si se acerca una llama, la fosfina se quema en el aire para dar ácido ortofosfórico:
PH3 (g) +
2 O2 (g) ![]() H3PO4 (l)
H3PO4 (l)
PH3 |
NH3 |
|
|---|---|---|
| Energía media enlace E-H (kJ·mol-1) | 322 |
391 |
| Ángulo de enlace H–E–H | 93.7 |
106.6 |
| Punto de fusión | -87.7 |
-33.35 |
| Afinidad protónica en gas (kJ·mol-1) | 770 |
866 |
| Propiedades | Base de Brönsted muy débil. A pesar de ello puede reaccionar con ácidos fuertes para dar sales de fosfonio (PH4+) | Base de Brönsted débil |
| No forma enlaces de hidrógeno | Si que forman enlaces de hidrógeno |
Obtención de PH3
Se prepara convenientemente de diferentes formas:
Hidrólisis del fosfuro cálcico
Ca3P2 + 6 H2O ![]() 2 PH3 + 3 Ca(OH)2
2 PH3 + 3 Ca(OH)2
Reducción con hidruros
PCl3 + 3 LiH ![]() PH3 + 3 LiCl
PH3 + 3 LiCl
Hidrólisis alcalina de P4
P4 + 3 KOH + 3 H2O
![]() PH3 + 3 KH2PO2
PH3 + 3 KH2PO2
En la síntesis se puede producir trazas de P2H4, análogo a la hidracina. Es un compuesto muy inestable y reactivo en cuya presencia la fosfina se incendia a temperatura ambiente.
PH3 + 2 O2 ![]() H3PO4
H3PO4
La arsina, AsH3, es mucho menos estable que la fosfina (se descompone rápidamente por el calor para dar As metal) y ya no tiene carácter de base.
Sales de fosfonio
Se pueden obtener diferentes haluros de fosfonio PH4+X- pero sólo el de yodo es estable por encima de 0ºC.